2025年9月3日,普林斯頓大學康毅濱教授團隊,在國際期刊Cell(IF:45.5)發表了題為“Tumors hijack macrophages for iron supply to promote bone metastasis and anemia"的研究性論文。該研究揭示,癌細胞通過“劫持"富含鐵的巨噬細胞以獲取鐵元素,導致了骨髓中缺乏生成健康紅細胞所需的鐵元素,使紅細胞處于未成熟狀態,從而導致貧血。此外,這些癌細胞還會模擬成紅細胞,從而在骨組織的低氧環境中維持增殖與存活。這些發現為開發減緩或阻止骨轉移的同時緩解常常伴隨骨轉移出現的嚴重貧血的療法開辟了新途徑。

骨骼是一種重要的器官,它為身體提供結構支撐,其內部的骨髓則參與造血。然而,骨骼也是癌癥轉移的常見部位,骨髓成為轉移瘤生長的肥沃土壤。因此,骨髓兼具造血功能核心區和轉移灶富集區的雙重生理特征。臨床上骨轉移患者常伴隨貧血現象,但其潛在關聯機制長期不明。約70%的晚期乳腺癌患者會發生骨轉移,此類轉移通常難以治療且患者預后較差。雖然雙膦酸鹽和地諾單抗等靶向溶骨細胞的藥物能夠通過調節骨重塑過程骨轉移治療,但僅能延緩疾病進展,無法實現治愈。骨轉移發生率高、并發癥多,給患者、護理人員及醫療系統均帶來了沉重的臨床負擔。因此,深入探索骨轉移的機制并開發相應治療策略,為應對這一未滿足的臨床需求具有重要意義。
研究團隊采用創新的體內轉移生態位標記系統,結合分泌型脂溶性mCherry和單細胞RNA測序技術,鑒定出一類高度特化的VCAM1? CD163? CCR3?富含鐵的巨噬細胞 (Iron-rich macrophage, iMac) 在骨轉移灶中異常聚集并緊密圍繞在癌細胞周圍。這些在紅細胞島中負責鐵轉運以支持紅細胞生成的巨噬細胞,在乳腺癌骨轉移小鼠模型中表現出向腫瘤區域的空間重分布。普魯士藍染色顯示鐵富集巨噬細胞在腫瘤-基質界面顯著積累,而紅系造血區域鐵可用性降低。
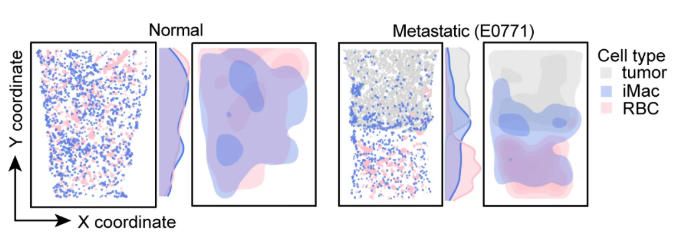
在健康骨髓中,這群iMac位于成紅細胞島(erythroblast island,EBI)中央,作為“保育細胞"為環繞其周圍的成紅細胞(紅細胞前體)提供鐵元素,以支持血紅素和血紅蛋白的合成,從而使紅細胞具備攜氧和輸氧功能。然而,在骨轉移發生時,腫瘤通過分泌IL-34和CCL5等信號分子將此類巨噬細胞大量招募至腫瘤區域,致使正常成紅細胞島數量顯著減少,可用于紅細胞生成的鐵供應降低。此外,被腫瘤利用的巨噬細胞還喪失了支持紅細胞終末成熟的能力(如細胞核的排出),進一步阻礙紅細胞發育,加劇貧血的發生。
研究表明,通過在小鼠模型中清除該類巨噬細胞可顯著抑制乳腺癌骨轉移進程。體外共培養實驗顯示,iMac能夠促進乳腺癌細胞增殖。通過鐵螯合劑處理、敲低腫瘤細胞中的轉鐵蛋白受體(CD71/Tfrc)或抑制巨噬細胞鐵輸出蛋白(Ferroportin/Slc40a1)以阻斷鐵傳遞后,巨噬細胞對腫瘤生長的支持作用明顯減弱。此外,在巨噬細胞中特異性敲除鐵輸出蛋白也可顯著延緩小鼠體內骨轉移的進展。
研究揭示了腫瘤細胞在缺氧骨髓環境中的特殊適應策略。單細胞轉錄組顯示骨轉移腫瘤細胞上調血紅素合成酶同時下調血紅素加氧酶HMOX1。值得注意的是,這些細胞通過GATA1介導的β-珠蛋白(HBB)表達獲得類成紅血細胞特征。這種表型可塑性使腫瘤細胞能將劫持的鐵用于血紅蛋白合成,增強其在缺氧骨髓環境中的存活能力。與鐵循環巨噬細胞共培養可放大缺氧-HBB軸效應,提示存在鐵可用性促進珠蛋白合成、進而加速鐵獲取的正反饋循環。
研究團隊在骨轉移患者的單細胞測序數據和組織切片分析中進一步證實,類似的富含鐵的巨噬細胞不僅存在于乳腺癌骨轉移灶,也見于肺癌和腎癌等其他腫瘤的骨轉移病灶中。這一發現提示,劫持含鐵巨噬細胞可能是多種癌癥類型發生骨轉移的共同機制。此外,乳腺癌細胞中HBB表達水平升高與骨轉移風險增加顯著相關。
總的來說,骨轉移的癌細胞通過“竊取" EBI 巨噬細胞的鐵,導致骨髓中缺乏生成健康紅細胞所需的鐵,使紅細胞處于未成熟狀態,從而導致患者貧血。此外,癌細胞還會將“竊取"的鐵用于自身,它們通過模擬紅細胞來適應骨髓環境。在一種名為 GATA1 的血細胞轉錄因子的引導下,癌細胞開始產生血紅蛋白,這與紅細胞中的血紅蛋白一樣,同樣負責運輸氧氣。這種“紅細胞擬態"使腫瘤能夠在骨組織的缺氧的環境中便于成長。
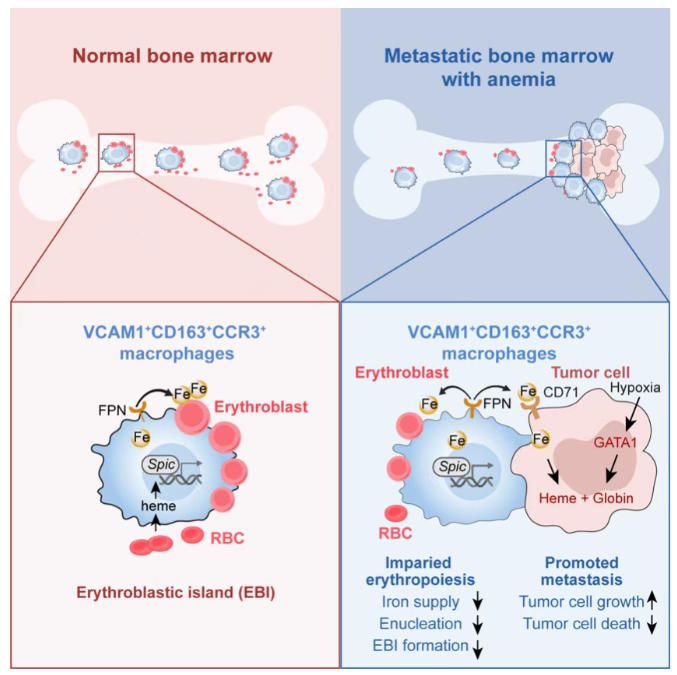
該研究的核心發現:
1.EBI 巨噬細胞被招募至骨轉移微環境;
2.EBI 巨噬細胞通過向腫瘤細胞轉運鐵來促進轉移;
3.將鐵的供應從成紅細胞轉移到腫瘤細胞會促進貧血;
4.腫瘤細胞通過模擬紅細胞來適應骨組織缺氧的微環境。
荷蘭Liposoma的巨噬細胞清除劑Clodronate Liposomes,氯膦酸鹽脂質體,廣泛用于體內單核巨噬細胞清除,頻頻登刊Cell,Nature和Science。如果您也在研究巨噬細胞,需要訂購巨噬細胞清除劑劑,就可以隨時聯系大中華辦事處靶點科技(Target Technology),專業技術團隊給您巨噬細胞清除提供整套解決方案。
原始文獻
Han, Yujiao et al. Tumors hijack macrophages for iron supply to promote bone metastasis and anemia. Cell, September 03, 2025.